定制合成 Custom synthesis
联系方式 Contact Us
多肽是由多个氨基酸经过肽键衔接而构成的一类化合物,普遍存在于生物体内,迄今在生物体内发现的多肽已达数万种。多肽在调理机体各系统、器官、组织和细胞的功用活动以及在生命活动中发挥重要作用,并且常被应用于功用剖析、抗体研讨、药物研发等范畴。随着生物技术与多肽合成技术的日臻成熟,越来越多的多肽药物被开发并应用于临床。
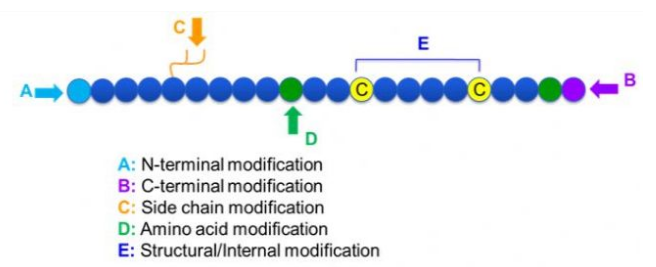
多肽修饰品种繁多,能够简单划分为后修饰和过程修饰(应用衍生化的氨基酸修饰),从修饰位点不同则可分为N端修饰、C端修饰、侧链修饰、氨基酸修饰、骨架修饰等(图1)。作为一种改动肽链主链构造或侧链基团的重要手腕,多肽修饰可有效改动肽类化合物的理化性质、增加水溶性、延长体内作用时间、改动其生物散布情况、消弭免疫原性、降低毒反作用等。本文主要引见几种最主要的多肽修饰战略及特性。
1、环化
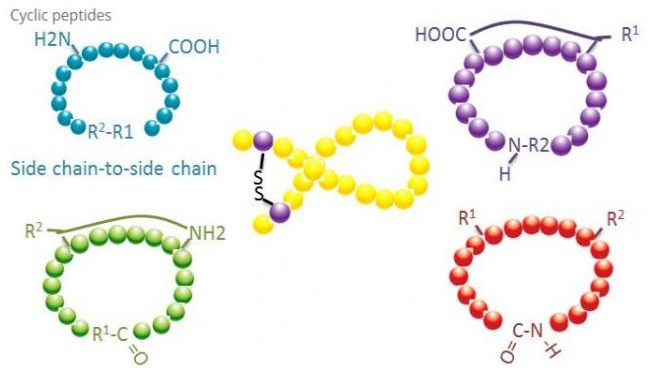
环肽在生物医学中具有诸多应用,而且许多具有生物活性的自然多肽都是环状多肽。由于环肽常常比线性肽更具有刚性,因而它们抵消化系统具有极强的抵御力,能够在消化道中存活,并且对靶受体表现出更强的亲和力。环化是合成环状多肽最直接的途径,特别关于构造骨架较大的多肽。依据环化方式能够分为侧链-侧链式、终端-侧链式、终端-终端式(头尾相连式)。
(1)侧链-侧链式(sidechain-to-sidechain)
侧链-侧链式环化最常见类型是半胱氨酸残基间的二硫桥接,引入这种环化的办法是经过一对半胱氨酸残基脱维护然后氧化构成二硫键。经过选择性地移除巯基维护基能够完成多环的合成。环化既能够在解离后的溶剂里完成,也能够在解离前的树脂上完成。由于树脂上的多肽不易构成可环化的构象,因而在树脂上环化可能要比在溶剂中环化低效。侧链-侧链式环化的另一品种型是在门冬氨酸或谷氨酸残基与根底氨基酸之间构成酰胺构造,它请求多肽无论是在树脂上还是解离后,侧链维护基都必需可以选择性移除。第三种侧链-侧链式环化是经过酪氨酸或对羟基苯甘氨酸构成联苯醚。自然产物中这品种型的环化只在微生物产物中存在,而且环化产物常常具有潜在药物价值。制备这些化合物需求共同的反响条件,因而不常用于常规多肽的合成。
(2)终端-侧链式(terminal-to-sidechain)
终端-侧链式环化通常触及C末端与赖氨酸或鸟氨酸侧链的氨基,或者N末端与门冬氨酸或谷氨酸侧链。还有一些多肽环化是经过末端C与丝氨酸或苏氨酸侧链构成醚键而构成。
(3)终端-终端式或头尾相连式(head-to-tail)
链状多肽能够在溶剂中环化或者固定在树脂上经过侧链环化。在溶剂中环化应该用低浓度的多肽以防止多肽的低聚反响。头尾相连式合成环状多肽的产率取决于链状多肽的序列。因而,在大范围制备环状多肽前,首先应该创立可能的链状先导多肽库,然后停止环化以寻觅能到达最佳结果的序列。
2、N-甲基化
N-甲基化最初呈现在自然多肽中,并被引入到多肽合成中以阻止氢键的构成,进而使得多肽愈加耐受生物降解和肃清。应用N-甲基化的氨基酸衍生物合成多肽是最主要的办法,另外也可应用N-(2-硝基苯磺酰氯)多肽-树脂中间体与甲醇停止Mitsunobu反响,该办法已被用于制备含有N-甲基化氨基酸的环状多肽库。
3、磷酸化
磷酸化是自然界中最常见的翻译后修饰之一。在人类细胞中,超越30%的蛋白质被磷酸化。磷酸化,特别是可逆磷酸化,在控制许多细胞过程中起重要作用,如信号转导、基因表达、细胞周期和细胞骨架调理以及细胞凋亡。
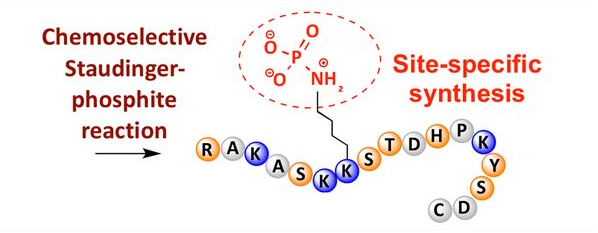
磷酸化能够在各种氨基酸残基上察看到,但最常见的磷酸化目的是丝氨酸、苏氨酸和酪氨酸残基。磷酸酪氨酸、磷酸苏氨酸和磷酸丝氨酸衍生物既可在合成中引入到多肽也可在多肽合成以后构成。运用可选择性移除维护基团的丝氨酸、苏氨酸和酪氨酸残基能够完成选择性磷酸化。一些磷酰化试剂也可经过后修饰在多肽中引入磷酸基团。近年来,有学者运用化学选择性的Staudinger-亚磷酸酯反响完成了赖氨酸的位点特异性磷酸化(图3)
4、豆蔻酰化和棕榈酰化
用脂肪酸酰化N末端能够让多肽或蛋白质与细胞膜分离。N末端上豆蔻酰化的序列能够使Src家族的蛋白激酶和逆转录酶Gaq蛋白靶向分离细胞膜。应用规范的偶联反响即可将豆蔻酸衔接到树脂-多肽的N末端,生成的脂肽可在规范条件下解离并经过RP-HPLC纯化。
5、糖基化
糖肽类如万古霉素和替考拉宁是治疗耐药细菌感染的重要抗生素,其他糖肽常被用于刺激免疫系统。另外,由于很多微生物抗原是糖基化的,因而研讨糖肽对进步感染的治疗效果具有重要意义。另一方面,有研讨发现肿瘤细胞细胞膜上的蛋白质表现出异常的糖基化,这使得糖肽在癌症和肿瘤免疫防御研讨中也发挥着重要作用。糖肽的制备普通应用Fmoc/t-Bu办法。糖基化残基,比方苏氨酸和丝氨酸常经过五氟苯酚酯活化的Fmoc维护糖基化氨基酸引入到多肽中。
6、异戊二烯化
异戊二烯化发作在C末端左近侧链上的半胱氨酸残基。蛋白质的异戊二烯化能够进步细胞膜亲和性,构成蛋白质-蛋白质互相作用。异戊二烯化的蛋白质包括酪氨酸磷酸酶、小GTP酶、协同伴侣分子、核纤层和着丝粒分离蛋白。异戊二烯化的多肽能够应用树脂上的异戊二烯化办法或者引入半胱氨酸衍生物制备。
7、聚乙二醇(PEG)修饰
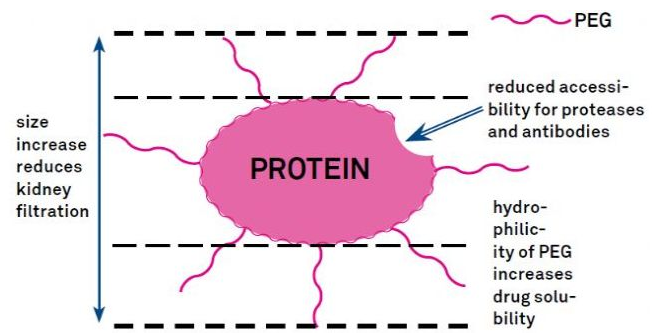
PEG修饰可用于改善蛋白水解稳定性、生物散布和肽的溶解度。在多肽上引入PEG链能够改善它们的药理性质,也能够抑止多肽被蛋白水解酶水解。PEG多肽比普通多肽更容易经过肾小球毛细血管截面,大大减少肾肃清率。由于PEG多肽在体内的有效半衰期延长,因而运用更低剂量、更低频度的多肽药物便能够维持正常治疗程度。但PEG修饰也存在负效应。大量PEG在阻止酶降解多肽的同时也会减少多肽与目的受体的分离。但PEG多肽的低亲和力通常被其更长的药动学半衰期抵消,经过在体内存在更久,PEG多肽有更大可能性被目的组织吸收。因而,PEG聚合物的规格应该针对最佳结果停止最优化设计。另一方面,由于肾肃清率降低,PEG多肽会在肝脏累积形成大分子综合征。因而,当多肽用于药物测试时需求愈加慎重地设计PEG修饰。
PEG修饰剂常见的修饰基团大致可总结如下:氨基(-Amine)-NH2,氨甲基-CH2-NH2,羟基-OH,羧基-COOH,巯基(-Thiol)-SH,马来酰亚胺-MAL,琥珀酰亚胺碳酸酯-SC,琥珀酰亚胺乙酸酯-SCM,琥珀酰亚胺丙酸酯-SPA,N-羟基琥珀酰亚胺-NHS,丙酸基-CH2CH2COOH,醛基-CHO(如丙醛-ALD,丁醛-butyrALD),丙烯酸基(-Acrylate)-ACRL,叠氮基-Azide,生物素基-Biotin,荧光素基-Fluorescein,戊二酸基-GA,酰肼基-Hydrazide,炔基-Alkyne,对甲苯磺酸酯基-OTs,琥珀酰亚胺琥珀酸酯-SS等。带有羧酸的PEG衍生物能够与N末端的胺或者赖氨酸侧链停止偶联。氨基活化的PEG能够与门冬氨酸或者谷氨酸侧链偶联。MAL活化的PEG能够与完整脱维护的半胱氨酸侧链的硫醇停止偶联[11]。PEG修饰剂常见分类如下(注:mPEG即methoxy-PEG,CH3O-(CH2CH2O)n-CH2CH2-OH):
(1)直链PEG修饰剂
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2)双官能团PEG修饰剂
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3)分枝形PEG修饰剂
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8、生物素化
生物素能够与亲和素或者链霉亲和素有力分离,分离强度以至接近共价键。生物素标志的肽通常用于免疫测定,组织细胞化学和基于荧光的流式细胞术。标志的抗生物素抗体也能够用来分离生物素化多肽。生物素标志常衔接在赖氨酸侧链或者N末端。通常在多肽和生物素之间运用6-氨基己酸作为纽带,纽带可以灵敏分离底物,并且在有空间位阻的状况下能分离地更好。
9、荧光标志
荧光标志可用于追踪活细胞内多肽,也可用于研讨酶和作用机制。色氨酸(Trp)带有荧光,因而能够被用于内在标志。色氨酸的发射光谱取决于外围环境,随着溶剂极性降低而降低,这种性质关于检测多肽构造和受体分离很有用途。色氨酸荧光能够被质子化的门冬氨酸和谷氨酸淬灭,这可能会限制其运用。丹磺酰氯基团(Dansyl)与氨基分离时具有高度荧光,也常被用于氨基酸或蛋白质的荧光标志。
荧光共振能量转换(FRET)对酶的研讨非常有用,应用FRET时,底物多肽常含有一个荧光标志基团和一个荧光淬灭基团。标志的荧光基团会被淬灭剂经过非光子能量传送淬灭。当多肽从所研讨的酶上解离下来,标志基团就会发射荧光。
10、笼形多肽
笼形多肽有光学移除性的维护基,光学移除性维护基能够屏蔽多肽与受体的分离。当遭到UV映照时,多肽会被活化,恢复与受体的亲和力。由于这种光学活化能够依据时间、振幅或者位置来控制,因此笼形多肽能够被用于研讨细胞内发作的反响。最常用于笼形多肽的维护基是2-硝基苄基及其衍生物,它们可在多肽合成中经过维护的氨基酸衍生物而引入。曾经开展的氨基酸衍生物有赖氨酸、半胱氨酸、丝氨酸和酪氨酸。而门冬氨酸和谷氨酸衍生物由于在多肽合成和解离过程中很容易环化,因而并不常用。
11、多聚抗原肽(MAP)
短肽通常不具有免疫性,必需和载体蛋白耦合才干产生抗体。多聚抗原肽(MAP)由多个衔接到赖氨酸核的相同多肽构成,能特异性表达高效免疫原,可用来制备肽-载体蛋白耦联体。MAP多肽能够在MAP树脂上应用固相合成法分步合成。但是,不完好的耦合会在一些分支上产生丢失或截断肽链,因此表现不出本来MAP多肽的性质。作为替代性的办法,多肽能够单独制备和纯化然后再耦联到MAP上。衔接到多肽中心上的多肽序列是明白的,并且很容易经过质谱表征。
结语:
多肽修饰是一种设计多肽的重要手腕,经过化学修饰的多肽不只能够维持较高的生物活性, 而且可以有效地防止免疫原性和毒性方面的缺陷,同时化学修饰能够赋予多肽一些新的优秀性能。近年来,应用C-H活化的手腕对多肽停止后期修饰的办法也得到了迅猛的开展,并获得了许多重要成果。
原创文章如有转载,请注明出处“本文首发于固拓多肽合成生物科技有限公司(www.gotopbio.com)”
本公司的所有产品仅用于科学研究或者工业应用等非医疗目的,不可用 于人类或动物的临床诊断或治疗,非药用,非食用。